2024년 다발경화증 진단 기준 개정
글_권순욱(인하대병원 신경과)
1. 서론
2017년 개정된 다발경화증 McDonald criteria가 발표된 후 진단 기준이 개정되어 곧 새로이 발표될 예정이다. 아직 새로운 진단 기준에 대한 논문이 발표되지는 않았으나 2024년 제40회 유럽다발경화증학회(ECTRIMS 2024)에서 발표된 내용을 바탕으로 변경이 될 부분들을 미리 살펴보고자 한다. 이번 진단 기준의 개정은 다발경화증 가능성이 높은 환자에서 조기에 다발경화증을 진단하고 치료를 할 수 있도록 제안되었으며, 또한 오진을 줄이기 위해 특이도를 높이기 위한 바이오마커들(biomarkers)도 새로이 추가된 것이 특징이겠다.
이번 진단 기준을 마련하기 위해 16개국에서 55명의 전문가들 의견을 수렴하였다. 이 중 17명은 이전 진단 기준을 개정할 때 참여하였으며 38명은 이번에 진단 기준을 정립할 때 새로이 참여를 하였다.
2. 일반적인 원칙 (General principles)

일반적인 원칙에서는 기존에 잘 알려진 부분들에 대해서 다시 공고히 하였다. 다발경화증은 배제진단을 원칙으로 하며, 진단을 위해서는 뇌와 척수 자기공명영상(magnetic resonance imaging, MRI) 소견이 매우 중요하다. 특히, 오진이나 과소진단이 환자에게 부정적인 영향을 끼칠 수 있으므로, 전형적인 병변 소견으로 판단을 하는 것을 원칙으로 하며, 주기적으로 재평가하는 것을 권장하고 있다.
3. 제안된 개정 사항들 (Proposed revisions)
1) 영상단독증후군(radiologically isolated syndrome, RIS)에서 다발경화증의 진단

RIS는 임상적 증상없이 뇌 혹은 척수 MRI에서 다발경화증을 시사하는 영상 소견을 보이는 경우를 의미한다. 2009년 RIS 진단 기준인 2023년 새로운 개정되어 제시된 바 있다. 2023 RIS 진단 기준에서는 2009년 진단 기준에 부합하거나 혹은 한 개 이상의 전형적인 탈수초 병변이 피질곁(juxtacortical), 뇌실주위(periventricular), 척막밑(infratentorial), 척수(spinal) 중 한 군데 이상에서 위치하면서, 아래 3가지 기준 중에 2개 이상을 만족하는 경우 RIS로 진단하도록 제시하였다. (① 뇌척수액검사에서 올리고클론띠(oligoclinal bands, OCBs) 확인, ② 적어도 하나 이상의 척수 병변, ③ 추적 MRI 영상에서 하나 이상의 새로운 T2강조 병변이나(T2-weighted hyperintensities)나 조영증강되는 병변(gadolinium enhancement)의 확인)
RIS 환자들을 추적 관찰한 연구에서 10년이 지난 경우 약 51%에서 다발경화증으로 진단되었으며, ECTRIMS 2024에서 발표된 연구에 따른 15년까지 추적 관찰하였을 때, 약 72%에서 다발경화증으로 진단되었다. 최근 RIS에서 다발경화증으로 진행하는 것에 대한 약물 치료의 효과를 보는 두 가지 연구들이 발표된 바가 있는데 (teriflunomide의 효과를 확인하기 위한 TERIS study, dimethyl fumarate의 효과를 확인하기 위한 Arise study), 두 연구 모두 약물 치료를 시작한 환자군이 그렇지 않은 환자군에 비해 다발경화증으로 진행하는 위험이 낮은 것으로 나타나 RIS 환자들에서도 치료의 필요성이 제시되었다. 이번 개정 사항에서는 RIS 환자들 중에 1) 공간파종(dissemination in space, DIS)과 시간파종(dissemination in time, DIT)을 만족하는 경우, 2) DIS를 만족하고 뇌척수액검사에서 OCB가 확인되는 경우, 3) DIS를 만족하는 환자들 중, 6개 이상의 중심정맥신호(central vein sign, CVS)가 확인되는 경우 임상적 증상 발생까지 기다리지 않고 다발경화증으로 진단을 하는 것을 제안하였다.
2) 5번째 병터위치(topography)로의 시신경

시신경염은 임상단독증후군의 25-35%를 차지하며, 질병 이환기간에 따라 다소 차이는 있으나 증상이 있는 눈의 경우 70-100%, 증상이 없는 눈에서도 8~70%에서 시신경의 침범이 확인되었다. 또한, 시신경염이 있으면서 뇌척수액에서 OCBs가 확인되면, 다발경화증 위험이 5.1배 증가하며, 시신경과 임상적으로 증상이 없는 뇌병변이 MRI에서 확인되면 다발경화증의 11.3배로 증가한다. 또한, 2017 McDonald criteria를 기준으로 DIS와 DIT를 만족할 때 병터위치에 시신경을 추가한 경우, 다발경화증 진단에 있어 특이도(specificity)의 저하 없이 민감도(sensitivity)와 정확도(accuracy)가 증가하였다.
이러한 연구결과들의 바탕으로 이번 개정에서는 시신경이 새로운 병터위치로 포함되었다. 이는 다른 원인으로 설명이 어려운 시신경의 침범이 MRI, 시각유발전위(full field pattern reversal visual evoked potential), 빛간섭단층촬영(optical coherence tomography)에서 확인되는 경우 시신경의 침범이 있는 것으로 제안하였다.
3) 유리경쇄-카파(Kappa free light chain, kFLC)

이번 개정에서 또 하나의 특징은 그 동안 많은 연구들이 진행된 바이오마커들이 적극적으로 진단기준에 포함한 것이다. kFLC는 B림프구가 항체를 형성하고 분비할 때 같이 분비가 되므로 OCBs와 마찬가지로 뇌척수액 내의 항체 형성을 시사하는 지표로 이용될 수 있다. 약 87% 다발경화증 환자들에서 kFLC가 OCBs와 동시에 존재하였다. 32개의 연구를 분석한 메타연구에서는 다발경화증 진단에서 있어서 kFLC이 OCB와 유사한 민감도나 특이도를 보였다. kFLC는 척수강내의 IgG 클론성(clonality)이나 IgG 합성 패턴(IgG synthesis patterns)은 알 수는 없으나 OCB에 비해 쉽고 빠르게 검사를 할 수 있으며, 비용 효율적이고, 정량적이며 해석이 어렵지 않다는 장점이 있다. 기존 연구들을 바탕으로 이번 개정에서는 kFLC가 OCB를 대체할 수 있는 바이오마커로 제안하였다.
4) 중심정맥신호(central vein sign, CVS)

중심정맥신호는 탈수초병변을 중심을 통과하는 정맥을 의미한다. 2016년에 North American Imaging in MS Cooperative(NAIMS)에서 이에 대한 기준을 제시하였다. T2*강조 영상에서 3mm이상 크기의 탈수초병변에서 직경 2mm이하의 저강도신호가 병변의 중심을 통과하며 이는 적어도 2개 이상의 수직영상(perpendicular)에서 확인되어야 한다. 병변의 40~50%에서 CVS가 확인되는 경우 다른 신경계 질환과 다발경화증이나 CIS를 감별하는데 매우 유용한 것으로 나타났다. 다만, 모든 병변을 다 확인하는 것은 많은 노력과 시간이 필요하기에 이번 개정에서는 “rule of 6”(10개의 병변에서 6개의 이상의 CVS가 보이는 경우)를 CVS가 양성으로 제시하여 진단기준에 포함하였다. 다만, 진단에 있어서 필 수적인 부분은 아니며, DIS를 만족하나 DIT를 만족하지 못하는 경우나 1군데에만 전형적인 병변이 관찰되는 경우 진단에 이용할 수 있다.
5) 상자성 테두리 병변 (Paramagnetic rim lesions, PRLs)

PRLs도 CVS와 마찬가지로 다른 신경계 질환들과 감별에 매우 유용한 영상 바이오마커이다. PRLs은 다발경화증 병변 가장자리에 있는 미세아교세포(대식세포)에 철분이 축적된 만성염증을 의미한다. 임상단독증후군과 재발완화형 및 진행형 다발경화증에서 최소 한 개 이상의 PRL이 50%이상에서 확인되었으며, 다른 신경계 질환에서는 1개 이상의 PRL이 있는 경우 10%미만으로 감별 진단의 지표로 매우 유용하다. 이번 개정에서는 CVS와 마찬가지로 다발경화증 진단에 필수적으로 필요한 조건은 아니지만 진단의 특이도를 높일 수 있는 지표로 이용하는 것을 제안하였다.
6) 개정된 DIS 기준 및 다발경화증 진단

앞서 언급한 내용들을 포함하여 제안된 다발경화증의 진단기준은 위에 기술하였다. 추가적으로 전형적인 증상과 병변이 4군데 이상의 병터에서 확인된다면 DIT를 만족하지 않고 뇌척수액 검사를 시행하지 않더라도 다발경화증을 진단할 수 있도록 제안하였다. 또한, 진행성 다발경화증의 경우 2개의 척수 병변이 있다면 DIS를 만족하는 것으로 제안하였다.
7) 소아 다발경화증

소아에서 다발경화증의 진단 기준은 성인과 동일한 기준을 적용하는 것으로 제안하였다. 다만 18세 미만의 경우, CVS의 기준으로 “rule of 6” 대신 “rule of 50%”를 제안하였으며, 12세 미만에서는 MOG-IgG의 검사를 제안하였다.
8) 일차진행다발경화증 (Primary Progressive MS, PPMS)

PPMS의 경우 이전과 마찬가지로 12개월 이상의 지속적인 임상적으로 악화가 있어야 하며, 그 외의 사항들은 재발완화다발경화증과 마찬가지로 하나의 프레임워크에서 진단하는 것을 제시하였다. 또한, 2개 이상의 척수 병변이 있는 경우 DIS를 만족하는 것으로 제안하였다.
9) 감별 진단에 대한 강조

일반 원칙에서도 다발경화증은 배제진단이 원칙임이 언급되었지만 특정한 상황에서는 추가적인 조건을 확인하는 것을 구체적으로 제안하였다. 다발경화증의 호발 연령은 20대에서 40대 사이이므로 50대 이후에 발생한 병변에 대해서는 다른 원인의 감별이 강조하였다. 또한, 편두통을 포함한 두통이 있는 환자에서 백질병변이 정상인에 비해 많으며, 혈관위험인자들이 많은 경우 뇌경색이나 소혈관질환의 가능성을 고려하여 다발경화증을 진단하기 위해서 추가적인 특징을 확인하는 것을 제안하였다.
이번 다발경화증 진단 기준 개정에서는 RIS 중 일부를 다발경화증으로 진단할 것을 제안하였고, 시신경이 새로운 병터위치로 포함되었으며, kFLC, CVS, PRL와 같은 바이오마커들이 포함되어 진단기준이 이전과 달리 매우 복잡해졌다. 이에 다발경화증 진단에 있어 하나의 프레임워크를 제시하였다.
1) 임상적 증상이 있는 경우
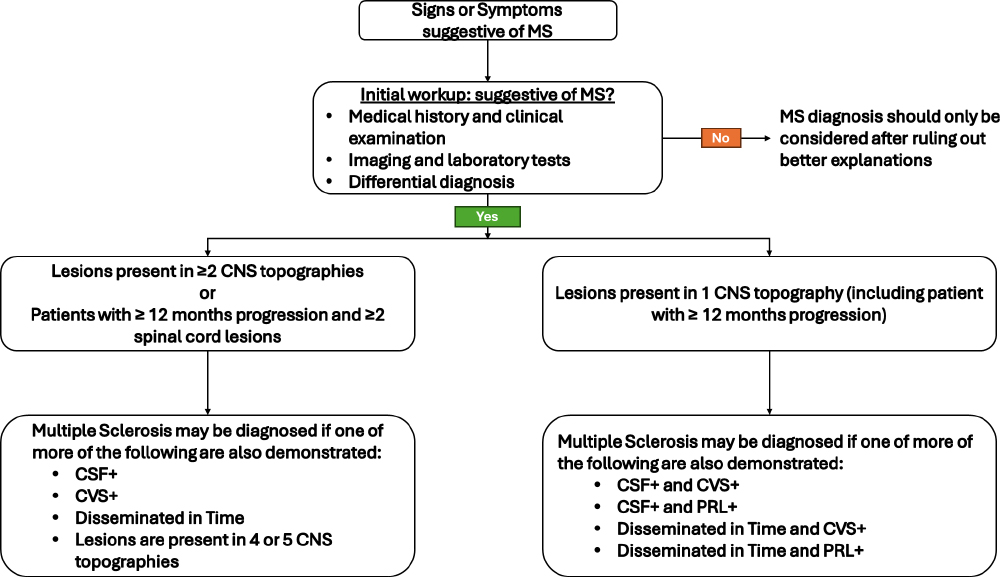
2) 우연히 병변이 확인된 경우
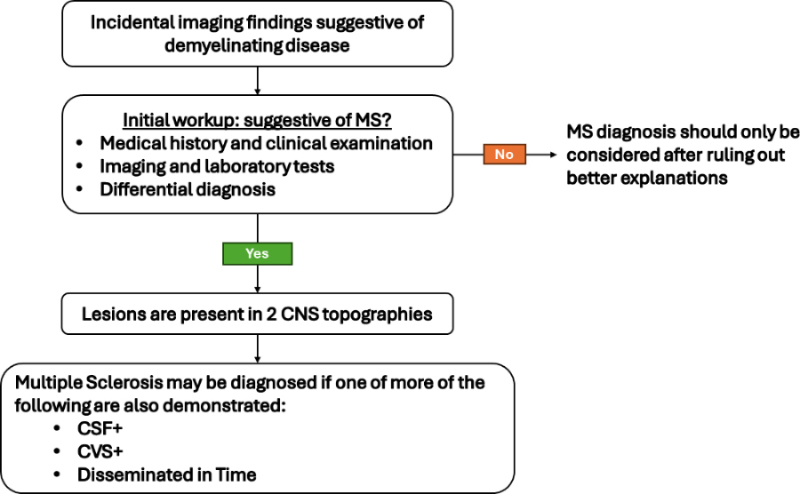
아직까지 2024 McDonald criteria에 대한 내용이 출판된 것은 아니므로 최종적으로 진단기준에 어떠한 내용이 반영되었는지 확인하는 것은 필요하겠다. 다만, 현재까지 발표된 내용에 의하면 다발경화증을 가능한 조기 발견하여 치료를 시작하고 신경학적 장애를 최소화하고자 하는 경향이 이번 개정에서도 반영이 된 것으로 보인다. 또한, 다른 질환들과 감별에 유용한 바이오마커들을 진단기준에 포함시키고, 특정 상황에서는 추가적인 기준 확인을 요함으로써 진단 특이도를 높였다.
다만, 2017년 다발경화증 진단 기준의 개정 이후 2018년도에 Multiple sclerosis 저널에서 Montalban 교수가 언급한 것처럼 OCB의 존재가 DIT를 만족하는 것은 아니며, 이번 개정에서도 kFLC, CVS, PRL의 바이오마커가 DIT를 입증한다는 의미는 아니다. 진단 기준으로서의 DIT의 중요성이 다소 줄었으나 진단이 명확치 않을 때에는 반복적인 영상 검사의 필요성을 상기함이 필요하겠다.
이번 진단 기준의 개정이 발표된 후로 실제 임상에서 진단 기준의 유효성 검증이 필요하겠으나, 다발경화증의 진단 시기가 빨라지고, 신경학적 장애를 줄일 수 있는 기점이 되기를 희망한다.

1. ECTRIMS 2024(McDonald Diagnostic Criteria | ECTRIMS)
2. Okuda DT, Kantarci O, Lebrun-Frenay C, et al. Dimethyl Fumarate Delays Multiple Sclerosis in Radiologically Isolated Syndrome. Ann Neurol. 2023;93(3):604-614. doi:10.1002/ana.26555
3. Brownlee WJ, Miszkiel KA, Tur C, Barkhof F, Miller DH, Ciccarelli O. Inclusion of optic nerve involvement in dissemination in space criteria for multiple sclerosis. Neurology. 2018;91(12):e1130-e1134. doi:10.1212/WNL.0000000000006207
4. Bsteh G, Hegen H, Altmann P, et al. Diagnostic Performance of Adding the Optic Nerve Region Assessed by Optical Coherence Tomography to the Diagnostic Criteria for Multiple Sclerosis. Neurology. 2023;101(8):e784-e793. doi:10.1212/WNL.0000000000207507
5. Cagol A, Cortese R, Barakovic M, et al. Diagnostic Performance of Cortical Lesions and the Central Vein Sign in Multiple Sclerosis. JAMA Neurol. 2024;81(2):143-153. doi:10.1001/jamaneurol.2023.4737
6. Filippi M, Rocca MA, Ciccarelli O, et al. MRI criteria for the diagnosis of multiple sclerosis: MAGNIMS consensus guidelines. Lancet Neurol. 2016;15(3):292-303. doi:10.1016/S1474-4422(15)00393-2
7. Hegen H, Arrambide G, Gnanapavan S, et al. Cerebrospinal fluid kappa free light chains for the diagnosis of multiple sclerosis: A consensus statement. Mult Scler. 2023;29(2):182-195. doi:10.1177/13524585221134217
8. Lebrun-Frenay C, Siva A, Sormani MP, et al. Teriflunomide and Time to Clinical Multiple Sclerosis in Patients With Radiologically Isolated Syndrome: The TERIS Randomized Clinical Trial. JAMA Neurol. 2023;80(10):1080-1088. doi:10.1001/jamaneurol.2023.2815
9. Okuda DT, Lebrun-Frenay C. Radiologically isolated syndrome in the spectrum of multiple sclerosis. Mult Scler. 2024;30(6):630-636. doi:10.1177/13524585241245306
10. Sati P, Oh J, Constable RT, et al. The central vein sign and its clinical evaluation for the diagnosis of multiple sclerosis: a consensus statement from the North American Imaging in Multiple Sclerosis Cooperative. Nat Rev Neurol. 2016;12(12):714-722. doi:10.1038/nrneurol.2016.166
11. Senel M, Tumani H, Lauda F, et al. Cerebrospinal fluid immunoglobulin kappa light chain in clinically isolated syndrome and multiple sclerosis. PLoS One. 2014;9(4):e88680. doi:10.1371/journal.pone.0088680
12. Suthiphosuwan S, Sati P, Absinta M, et al. Paramagnetic Rim Sign in Radiologically Isolated Syndrome. JAMA Neurol. 2020;77(5):653-655. doi:10.1001/jamaneurol.2020.0124
13. Toljan K, Daboul L, Raza P, et al. Diagnostic performance of central vein sign versus oligoclonal bands for multiple sclerosis. Mult Scler. 2024;30(10):1268-1277. doi:10.1177/13524585241271988
14. Meaton I, Altokhis A, Allen CM, et al. Paramagnetic rims are a promising diagnostic imaging biomarker in multiple sclerosis. Mult Scler. 2022;28(14):2212-2220. doi:10.1177/13524585221118677


























